Ein japanisches Sprichwort sagt: „Der erste Schluck ist ein Gast, der zweite ein Freund, der dritte ein Tyrann.“ Genau so entgleitet Kontrolle – erst unmerklich, dann gnadenlos. Für High-Performer ist das tückisch: Was als gelegentlicher Kick beginnt, frisst sich in Neurobiologie, Schlaf, Entscheidungsfähigkeit und letztlich Identität. Die gute Nachricht: Das Gehirn ist formbar. Mit klugen Routinen, Ernährung und mentalem Training lässt sich der Abstieg stoppen – und sogar umkehren.
Sucht ist kein moralisches Versagen, sondern eine erlernte Neuroadaptation. Wiederholte Reize überformen Belohnungskreise im Gehirn, besonders das mesolimbische SystemDopamin-gesteuertes Netzwerk, das Motivation und Belohnung steuert, die präfrontale KortexStirnhirnregion für Planung, Impulskontrolle und Entscheidungsfähigkeit und Stressachsen. Substanzen wie Alkohol, Cannabis, Stimulanzien oder Benzodiazepine verschieben die Balance zwischen Dopamin, GABA, Glutamat und Serotonin; der Alltag verliert Farbe, während der Suchtreiz Priorität gewinnt. Entscheidender Punkt: Neuroplastizität arbeitet in beide Richtungen. Dasselbe Prinzip, das Abhängigkeit formt, ermöglicht auch Erholung – durch gezielte Reize, Schlaf, Ernährung, Therapie und soziale Eingebundenheit.
Exzessiver Alkoholkonsum greift das zentrale Nervensystem an und ist mit Entzugssyndromen, Wernicke-Korsakow, Demyelinisierung und kognitiven Störungen verknüpft; genetische Varianten in Alkoholdehydrogenase und Aldehyddehydrogenase beeinflussen zusätzlich das Risiko [1]. Häufiger, hochpotenter Cannabiskonsum – besonders in der Adoleszenz – stört Hirnreifung und erhöht die Anfälligkeit für Psychosen, Angst, Depressionen und Cannabisabhängigkeit [2]. Bei diagnostizierter Cannabis-Use-Disorder zeigen Metaanalysen anhaltende Defizite in verbaler Lern- und Arbeitsgedächtnisleistung sowie Verarbeitungsgeschwindigkeit – Funktionen, die High-Performance unmittelbar tragen [3]. Tiermodelle bestätigen langanhaltende Verschaltungenstörungen zwischen Kortex und Striatum nach THC-Exposition, die soziale Interaktion und sensorische Filterung beeinträchtigen [4]. Stimulanzien wie MDMA oder Kokain können über die mitochondriale Calciumaufnahme zu oxidativem Stress, Energiekrisen und neuronalem Zelltod führen – ein leiser, aber tiefgreifender Verschleiß der neuronalen „Energiewerke“ [5]. Unkontrollierter Benzodiazepin-Gebrauch erhöht Sturz-, Delir- und Abhängigkeitsrisiko; besonders bei Älteren sind inadäquate Verordnungen häufig, Entzug ist jedoch mit kurzer kognitiver Therapie realistisch erreichbar [6].
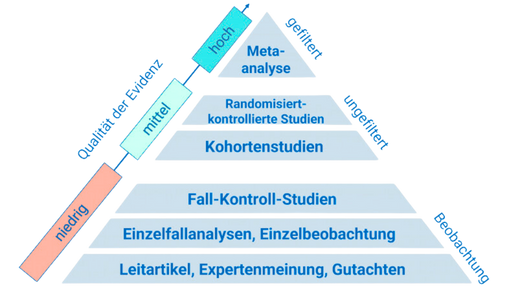
Mehrere Linien der Evidenz zeichnen ein konsistentes Bild: Eine große Übersichtsarbeit zu alkoholbezogener Neurologie beschreibt die zentrale Rolle von Neurotransmitter-Verschiebungen und genetischen Risikovarianten bei Alkoholabhängigkeit sowie strukturelle Schäden von Degeneration bis Demyelinisierung – ein Mechanismus, der erklärt, warum Leistungseinbußen oft trotz „funktionierendem“ Alltag auftreten [1]. Im Cannabiskontext zeigt die translational kombinierte Forschung aus Langzeit-Neuroimaging beim Menschen und Tiermodellen, dass frühe, häufige Exposition mit hoch-THC-Produkten die jugendliche Hirnreifung stören und Pfade zu Psychose, Angst und Cannabis-Use-Disorder bahnen kann; wichtig und ermutigend: Nicht alle Veränderungen sind irreversibel, was Prävention und frühe Intervention sinnvoll macht [2]. Ergänzend quantifiziert eine Metaanalyse bei Cannabis-Use-Disorder kleine bis moderate Defizite in 10 von 13 kognitiven Domänen, am stärksten in verbaler Erinnerung, Arbeitsgedächtnis und Verarbeitungstempo – genau jene Exekutivfunktionen, die High-Performer im Alltag maximal belasten [3]. Auf der Seite der Stimulanzien weist aktuelle Grundlagenforschung den mitochondrialen Calciumuniporter als Schlüsselknoten der Neurotoxizität aus; Ca2+-Überladung triggert oxidativen Stress und Apoptose. Das ist klinisch relevant, weil es zukünftige zielgerichtete Schutzstrategien – etwa selektive MCU-Inhibitoren – denkbar macht, auch wenn deren Langzeitsicherheit noch offen ist [5].
- Ernähren Sie sich ausgewogen mit Fokus auf Omega-3-Fettsäuren: Täglich 2–3 Portionen fettreichen Fisch (z. B. Lachs, Makrele) oder 1–2 EL Algen-/Leinöl integrieren. DHA/EPA nähren neuronale Membranen der präfrontalen Kortex und können Impulsivität und Stressreaktivität dämpfen – Faktoren, die Suchtpfade befeuern [7]. Bei Alkoholkonsum zeigen präklinische Daten, dass n-3-Fettsäuren synaptische Defizite abmildern und neuroinflammatorische Prozesse bremsen können; klinische Evidenz ist noch uneinheitlich, doch das Nutzen-Risiko-Profil ist günstig [8].
- Verbessern Sie Ihre Schlafhygiene: Ziel sind 7–9 Stunden konsistenter, tiefer Schlaf. Feste Schlafzeiten, dunkle, kühle Umgebung und 90 Minuten vor dem Zubettgehen Bildschirme meiden. Schlaf konsolidiert Gedächtnis und emotionale Regulation – Schutzfaktoren gegen Suchtdruck. Bei hartnäckigen Problemen können evidenzbasierte, nichtinvasive Neurostimulationen und verhaltenstherapeutische Schlafprogramme ergänzen; sie verbessern Schlafqualität und kognitive Funktionen, die Rückfallrisiken senken [9].
- Soziale Unterstützung aktiv aufbauen: Planen Sie wöchentliche „Accountability“-Termine mit Freunden oder in Recovery-Communities. Daten aus sportbasierten, nüchternen Communities zeigen: Wer zentral in einem unterstützenden Netzwerk steht, berichtet weniger psychische Belastung; periphere Positionen korrelieren mit höherem Distress [10]. Übersetzen Sie das in den Alltag: Treten Sie einer Gruppe bei, die Leistung ohne Substanzen feiert (z. B. Running Crew, CrossFit, Kletterhalle).
- Trainieren Sie kognitive Verhaltenstechniken (CBT): Täglich 10 Minuten für kognitive Umstrukturierung – automatische Gedanken identifizieren, Evidenz checken, realistische Alternativen formulieren. Metaanalyse: CBT reduziert transdiagnostisches Grübeln/Worry moderat bis stark; RNT-spezifische Module wirken am stärksten [11]. Digitale oder agentenbasierte CBT-Formate können akute Anspannung und Angst senken und die Veränderungsbereitschaft erhöhen – ideal als „Just-in-time“-Intervention [12]. Bei anhaltender Niedergeschlagenheit helfen modulare Programme (z. B. Metakognitives Training), ruminations- und schwarz-weiß-Denken gezielt zu entkoppeln – ein Hebel gegen Triggerverhalten [13].
Die nächsten Jahre werden zwei Hebel besonders vorantreiben: präzise Neuroprotektion – etwa über mitochondriale Zielstrukturen bei Stimulanzien-Schäden – und personalisierte, digitale CBT-Tools, die RNT in Echtzeit dämpfen [5] [11] [12]. Parallel deutet die Cannabisforschung auf ein „kritisches Fenster“ hin: frühe Prävention kann neurobiologische Pfade umlenken und kognitive Resilienz stärken – eine Einladung, Gesundheitsverhalten heute zu justieren [2] [3].
Dieser Gesundheitsartikel wurde mit KI-Unterstützung erstellt und soll Menschen den Zugang zu aktuellem wissenschaftlichem Gesundheitswissen erleichtern. Er versteht sich als Beitrag zur Demokratisierung von Wissenschaft – ersetzt jedoch keine professionelle medizinische Beratung und kann durch KI-generierte Inhalte einzelne Details vereinfacht oder leicht ungenau wiedergeben. HEARTPORT und seine Partner übernehmen keine Haftung für die Richtigkeit, Vollständigkeit oder Anwendbarkeit der bereitgestellten Informationen.